RNK komponenta telomeraze
| TERC | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Identifikatori | |||||||
| Alijasi | TERC | ||||||
| Spoljašnji ID | OMIM: 602322 GeneCards: TERC | ||||||
| Ortolozi | |||||||
| Vrste | Čovek | Miš | |||||
| Entrez |
|
| |||||
| Ensembl |
|
| |||||
| UniProt |
|
| |||||
| RefSeq (mRNA) |
|
| |||||
| RefSeq (protein) |
|
| |||||
| Location (UCSC) | n/a | n/a | |||||
| PubMed search | [1] | n/a | |||||
| Wikidata | |||||||
| |||||||
| Telomerazna RNK kičmenjaka | |
|---|---|
 | |
| Identifikatori | |
| Simbol | Telomerase-vert |
| Rfam | RF00024 |
| Drugi podaci | |
| RNK tip | Gen |
| Domain(i) | Eukariote; Virus |
| Telomerazna RNK trepljara | |
|---|---|
 | |
| Identifikatori | |
| Simbol | Telomerase-cil |
| Rfam | RF00025 |
| Drugi podaci | |
| RNK tip | Gen |
| Domain(i) | Eukariote |
| Telomerazna RNK Saccharomyces cerevisiae | |
|---|---|
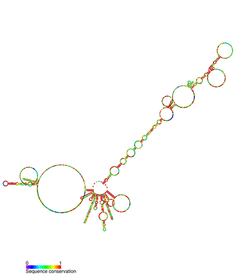 | |
| Identifikatori | |
| Simbol | Sacc_telomerase |
| Rfam | RF01050 |
| Drugi podaci | |
| RNK tip | Gen |
| Domain(i) | Eukariote |
RNK komponenta telomeraze, takođe poznata ka TERC, je RNK gen prisutan kod eukariota, koji je komponenta telomeraze, enzima koji produžava telomere.[2][3] TERC služe kao šabloni za telomernu replikaciju (reverznu transkripciju) posredstvom telomeraze. Telomerazne RNK se znatno razlikuju po sekvuenci i strukturi između kičmenjaka, trepljara i kvasaca, mada oni imaju zajedničku strukturu 5' pseudočvora u blizini sekvence šablona. Telomerazna RNA kičmenjaka ima 3' H/ACA domen sličan snoRNK.[4][5][6]
Funkcija
Telomeraza je ribonukleoproteinska polimeraza koja održava telomerne krajeve dodavanjem telomernih ponavljanja TTAGGG. Ovo ponavljanje varira među eukariotama. Enzim se sastoji od proteinske komponente (TERT) sa reverzno transkriptaznom aktivnošću, i RNK komponente, kodirane ovim genom, koja služi kao šablon za telomerno ponavljanje. Izaražavanje telomeraze ima ulogu u ćelijskom starenju, te je normalno zastupljeno u postnatalnim somatskim ćelijama u kojima se javlja progresivno skraćivanje telomera. Deregulacija izražavanja telomeraze u somatskim ćelijama može da doprinese onkogenezi. Studije na miševima sugeriraju da telomeraze takođe učestvuju u hromozomalnoj popravci, pošto do novo sinteze telomernih ponavljanja može doći pri dvolančanim prekidima.[7] Homolozi TERC se takođe mogu naći u Gallid herpes virusima.[8]
Klinički značaj
Mutacije ovog gena uzrokuju autosomalno dominantni diskeratosis kongenita, i mogu da budu asocirane sa delom slučajeva aplastične anemije.[7]
Reference
- ^ „Human PubMed Reference:”. National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Feng J, Funk WD, Wang SS, Weinrich SL, Avilion AA, Chiu CP, Adams RR, Chang E, Allsopp RC, Yu J (1995). „The RNA component of human telomerase”. Science. 269 (5228): 1236—41. PMID 7544491. doi:10.1126/science.7544491.
- ^ Jády BE, Richard P, Bertrand E, Kiss T (2006). „Cell Cycle-dependent Recruitment of Telomerase RNA and Cajal Bodies to Human Telomeres”. Mol. Biol. Cell. 17 (2): 944—54. PMC 1356602
 . PMID 16319170. doi:10.1091/mbc.E05-09-0904.
. PMID 16319170. doi:10.1091/mbc.E05-09-0904. - ^ McCormick-Graham, M; Romero DP (1995). „Ciliate telomerase RNA structural features”. Nucleic Acids Res. 23 (7): 1091–1097. PMC 306816
 . PMID 7739888. doi:10.1093/nar/23.7.1091.
. PMID 7739888. doi:10.1093/nar/23.7.1091. - ^ Lingner, J; Hendrick LL; Cech TR (1994). „Telomerase RNAs of different ciliates have a common secondary structure and a permuted template”. Genes Dev. 8 (16): 1984–1998. PMID 7958872. doi:10.1101/gad.8.16.1984.
- ^ Theimer CA, Feigon J (2006). „Structure and function of telomerase RNA”. Curr. Opin. Struct. Biol. 16 (3): 307—18. PMID 16713250. doi:10.1016/j.sbi.2006.05.005.
- ^ а б „Entrez Gene: TERC telomerase RNA component”.
- ^ Fragnet, L; Kut E; Rasschaert D (2005). „Comparative functional study of the viral telomerase RNA based on natural mutations”. J Biol Chem. 280 (25): 23502–23515. PMID 15811851. doi:10.1074/jbc.M501163200.
Literatura
- de Lange T, Jacks T (1999). „For better or worse? Telomerase inhibition and cancer”. Cell. 98 (3): 273—5. PMID 10458601. doi:10.1016/S0092-8674(00)81955-8.
- Marrone A, Dokal I (2007). „Dyskeratosis congenita: molecular insights into telomerase function, ageing and cancer”. Expert Reviews in Molecular Medicine. 6 (26): 1—23. PMID 15613268. doi:10.1017/S1462399404008671.
- Yamaguchi H (2007). „Mutations of telomerase complex genes linked to bone marrow failures”. Journal of Nippon Medical School = Nihon Ika Daigaku zasshi. 74 (3): 202—9. PMID 17625368. doi:10.1272/jnms.74.202.
- Zaug AJ, Linger J, Cech TR (1996). „Method for determining RNA 3' ends and application to human telomerase RNA”. Nucleic Acids Res. 24 (3): 532—3. PMC 145649
 . PMID 8602368. doi:10.1093/nar/24.3.532.
. PMID 8602368. doi:10.1093/nar/24.3.532. - Soder AI, Hoare SF, Muire S, et al. (1997). „Mapping of the gene for the mouse telomerase RNA component, Terc, to chromosome 3 by fluorescence in situ hybridization and mouse chromosome painting”. Genomics. 41 (2): 293—4. PMID 9143511. doi:10.1006/geno.1997.4621.
- Zhao JQ, Hoare SF, McFarlane R, et al. (1998). „Cloning and characterization of human and mouse telomerase RNA gene promoter sequences”. Oncogene. 16 (10): 1345—50. PMID 9546436. doi:10.1038/sj.onc.1201892.
- Mitchell JR, Wood E, Collins K (1999). „A telomerase component is defective in the human disease dyskeratosis congenita”. Nature. 402 (6761): 551—5. PMID 10591218. doi:10.1038/990141.
- Chen JL, Blasco MA, Greider CW (2000). „Secondary structure of vertebrate telomerase RNA”. Cell. 100 (5): 503—14. PMID 10721988. doi:10.1016/S0092-8674(00)80687-X.
- Wong KK, Chang S, Weiler SR, et al. (2000). „Telomere dysfunction impairs DNA repair and enhances sensitivity to ionizing radiation”. Nat. Genet. 26 (1): 85—8. PMID 10973255. doi:10.1038/79232.
- Mitchell JR, Collins K (2000). „Human telomerase activation requires two independent interactions between telomerase RNA and telomerase reverse transcriptase”. Mol. Cell. 6 (2): 361—71. PMID 10983983. doi:10.1016/S1097-2765(00)00036-8.
- Imoto I, Pimkhaokham A, Fukuda Y, et al. (2001). „SNO is a probable target for gene amplification at 3q26 in squamous-cell carcinomas of the esophagus”. Biochem. Biophys. Res. Commun. 286 (3): 559—65. PMID 11511096. doi:10.1006/bbrc.2001.5428.
- Vulliamy T, Marrone A, Goldman F, et al. (2001). „The RNA component of telomerase is mutated in autosomal dominant dyskeratosis congenita”. Nature. 413 (6854): 432—5. PMID 11574891. doi:10.1038/35096585.
- Pruzan R, Pongracz K, Gietzen K, et al. (2002). „Allosteric inhibitors of telomerase: oligonucleotide N3′→P5′ phosphoramidates”. Nucleic Acids Res. 30 (2): 559—68. PMC 99832
 . PMID 11788719. doi:10.1093/nar/30.2.559.
. PMID 11788719. doi:10.1093/nar/30.2.559. - Zhang RG, Zhang RP, Wang XW, Xie H (2004). „Effects of cisplatin on telomerase activity and telomere length in BEL-7404 human hepatoma cells”. Cell Res. 12 (1): 55—62. PMID 11942411. doi:10.1038/sj.cr.7290110.
- Yang Y, Chen Y, Zhang C, et al. (2002). „Nucleolar localization of hTERT protein is associated with telomerase function”. Exp. Cell Res. 277 (2): 201—9. PMID 12083802. doi:10.1006/excr.2002.5541.
- Chang JT, Chen YL, Yang HT, et al. (2002). „Differential regulation of telomerase activity by six telomerase subunits”. Eur. J. Biochem. 269 (14): 3442—50. PMID 12135483. doi:10.1046/j.1432-1033.2002.03025.x.
- Gavory G, Farrow M, Balasubramanian S (2002). „Minimum length requirement of the alignment domain of human telomerase RNA to sustain catalytic activity in vitro”. Nucleic Acids Res. 30 (20): 4470—80. PMC 137139
 . PMID 12384594. doi:10.1093/nar/gkf575.
. PMID 12384594. doi:10.1093/nar/gkf575. - Sood AK, Coffin J, Jabbari S, et al. (2003). „p53 null mutations are associated with a telomerase negative phenotype in ovarian carcinoma”. Cancer Biol. Ther. 1 (5): 511—7. PMID 12496479. doi:10.4161/cbt.1.5.167.
- Antal, M; Boros E; Solymosy F; Kiss T (2002). „Analysis of the structure of human telomerase RNA in vivo”. Nucleic Acids Res. 30 (4): 912–920. PMC 100349
 . PMID 11842102. doi:10.1093/nar/30.4.912.
. PMID 11842102. doi:10.1093/nar/30.4.912.
Spoljašnje veze
- GeneReviews/NCBI/NIH/UW entry on Dyskeratosis Congenita
- GeneReviews/NCBI/NIH/UW entry on Pulmonary Fibrosis, Familial
- EntrezGene page for TERC
- Rfam strana za Vertebrate telomerase RNA
- Rfam strana za Ciliate telomerase RNA
- Rfam strana za Saccharomyces telomerase
- p
- r
- u
i inicijacija
| Prokariotska (inicijacija) | |
|---|---|
| Eukariotska (priprema u G1 fazi) | Prereplikacioni kompleks: Kompleks prepoznavanja mesta početka (ORC1, ORC2, ORC3, ORC4, ORC5, ORC6) · Održavanje minihromozoma (MCM2 · MCM3 · MCM4 · MCM5 · MCM6 · MCM7) · CDC6 Autonomna replikaciona sekvenca Protein jednolančanog vezivanja (SSBP1, SSBP2, SSBP3, SSBP4) Primaza: PRIM1 · PRIM2 |
| Oba | Početak replikacije/Ori/Replikon Replikaciona viljuška (zaostajući i vodeći lanci) · Okazakijev fragment · Prajmer |
| Prokariotska (elongacija) | DNK polimeraza III holoenzim (dnaC, dnaE, dnaH, dnaN, dnaQ, dnaT, dnaX, holA, holB, holC, holD, holE) · Replizom · DNK ligaza · DNK stega · Topoizomeraza (DNK giraza) Prokariotska DNK polimeraza: DNK polimeraza I (Klenov fragment) |
|---|---|
| Eukariotska (sinteza u S fazi) | |
| Oba | Kretanje: Procesivnost · DNK ligaza |










